【全面解读】揭秘肿瘤转移:一场生命与死神的赛跑!

当癌细胞从原发部位悄然扩散,潜入血液和淋巴系统,在身体的未知角落安营扎寨,一场生命与死神的赛跑便悄无声息地展开。
肿瘤转移,这个医学界尚未完全攻克的难题,它背后的诱因和过程比人们想象得更为复杂和诡异。
它不仅仅是关于生与死的决战,更是一场身体内部的权力游戏,涉及到一系列精细调控的信号通路。从微观角度来看,肿瘤细胞的每一次迁徙,都是一场精心策划的“舞蹈”,舞步的每一个变化都受到严格调控。
这些调控者,就是肿瘤转移过程中起着关键作用的信号通路。它们如同城市的交通指挥系统,确保细胞之间的信息交流无误,同时也掌控着细胞的命运。
那么,这些信号通路究竟是何方神圣?它们又是如何协同工作,推动肿瘤的转移的呢?本篇内容为大家揭秘!
文献解读
最近,美国Memorial Sloan Kettering Cancer Center的Karuna Ganesh教授团队在顶尖期刊Cell上发表了一篇题为“Metastasis”的综述文章,详细总结了肿瘤转移研究的最新进展。

肿瘤转移是肿瘤细胞在远离其起源部位中生长的现象,这是肿瘤最致命的表现之一,也是肿瘤恶性转化发展的重要环节和治疗失败的主要原因。
绝大多数癌症患者因转移性疾病而非原发性肿瘤而死亡。目前关于肿瘤转移的成因有多种说法,但治疗手段非常有限。
以Metastasis为关键词搜索,2014-01至2023-12的文献有 260492 篇,文献年均发文量26050篇。如下图所示,2023达到年发文量顶峰33765篇,2020增长率最快为13.45%,提示该领域的研究得到快速发展,处于快速上升阶段。

2014-01至2023-12 Metastasis相关文献的年度发文趋势,文献计量学分析来自于citexs赛特新思网站(https://www.citexs.com/)。
肿瘤转移包括一系列生物学事件,其中来自原发肿瘤的细胞逐渐获得通过粘膜侵入深层组织的能力;通过血液、淋巴管或通过直接渗透到邻近结构;播撒远处器官;这些事件中的每一个都是由肿瘤细胞采用不同的表型细胞状态并在肿瘤环境中选择其周围的免疫和间质细胞以支持其生长和逃避免疫系统的能力推动的。
与原发肿瘤不同,转移性癌症通常可以通过手术和放射等局部治疗来治愈,转移性癌症是一种全身性疾病,影响多个器官,要么直接侵占器官并损害其功能,要么通过改变分泌物改变它们的新陈代谢,最终导致死亡。
在同一患者的原发和转移性疾病中,即使对系统治疗的反应也可能截然不同。由于转移性肿瘤对现有治疗方法的获得性耐药,临床上明显的转移仍然在很大程度上是不可治愈的,只有少数例外。在这里,研究者系统回顾了肿瘤转移的主要原理,并强调了开发更有效治疗转移性癌症的新机会。
肿瘤转移的三个阶段
肿瘤的转移是一个复杂的过程,主要包含以下三个阶段:
01
侵袭阶段
原位肿瘤细胞经历上皮细胞-间充质转化(EMT),增强其侵袭能力。这些细胞扩散到周围的组织,并迁移至血管或淋巴管附近。一旦到达这些管道,它们会穿透血管壁,进入循环系统,成为循环肿瘤细胞(CTCs)。
02
循环阶段
在循环阶段,血小板会直接附着在CTCs表面,形成“细胞微栓”(Micro-thrombi)。这种结构能够降低免疫系统对CTCs的识别和清除。
03
定植阶段
CTCs最终会在远端器官的“前转移灶”(Pre-metastatic niche)定植。这种“前转移灶”是在原位肿瘤组织分泌的细胞因子或外泌体的作用下形成的,它创造了一个有利于肿瘤细胞定植的环境,带有免疫抑制的炎性特征。

肿瘤转移原则
转移细胞在经历转移级联反应的每一步时,需要具备大量的特征。这些特征部分源自原发肿瘤,是癌基因被激活和抑癌基因受到破坏后,基因突变的产物。这些特征使得细胞能够不受控制地生存、增殖、自我更新、迁移和入侵。然而,即使具备这些致癌特征,离开原发肿瘤的大多数癌细胞也无法存活并形成远处转移。因此,转移成为了一个主要的进化瓶颈。
转移特异性特征的出现,可能是由于以下两种机制:
(1)从原发癌细胞群体中存在的遗传异质性中选择特定的克隆;
(2)离开原发肿瘤的细胞在不同转移阶段需求的非遗传动态适应。

在转移过程中发育和再生程序的共同选择
转移细胞重新激活正常胚胎发育和伤口愈合再生机制:
A
在动态平衡期间,组织特异性干细胞不断产生转运放大的祖细胞和成熟的分化细胞。在组织损伤时,分化的上皮细胞去分化,重新进入组织胎儿样的、损伤相关的瞬时祖细胞状态,可以分化为组织干细胞,然后分化为不同的分化细胞,恢复上皮的完整性。
B
在胚胎发育过程中,细胞的命运逐渐受到限制,其可塑性逐渐降低。然而,当组织受损时,那些原本命运受限的分化细胞会短暂地增加其可塑性。癌细胞在肿瘤进展过程中,为了适应各种压力,会采用发育和再生过程中前体细胞所使用的程序。然而,关于在大的肿瘤转移过程中,细胞是保持高度可塑性还是变得命运受限,目前尚不明确。
C
弥散型MICs采用高塑性状态。这些状态包括混合EMT状态、损伤相关的暂时性类祖细胞状态或免疫逃避休眠状态。在转移定植过程中,MICs可以再生表型不同的大转移肿瘤,这些肿瘤可以进入休眠或启动肿瘤生长,重新进入与原发肿瘤相似的状态(弹性),保持MIC样状态(变形),或经历谱系可塑性进入原发肿瘤中未发现的新细胞状态(转分化)。


转移性肿瘤微环境
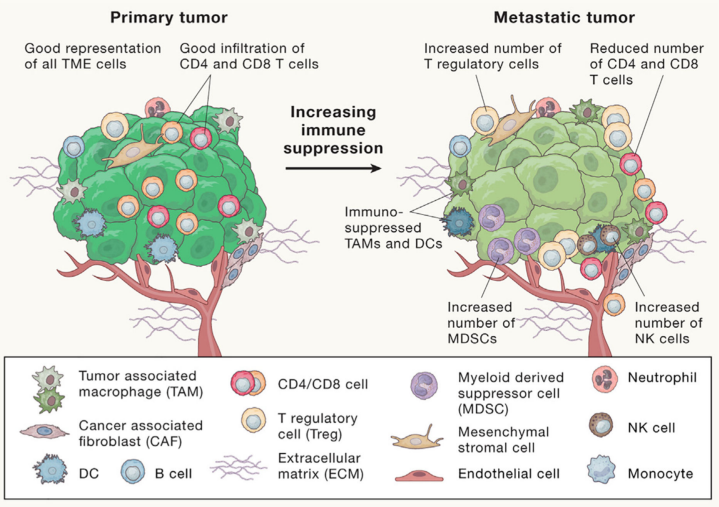
TME的组成和选择对肿瘤的生长和进展是必不可少的.TME的主要成分是先天和获得性免疫系统以及基质细胞:组织驻留和骨髓来源的巨噬细胞,极化为免疫抑制TAM、单核细胞、髓系来源的抑制细胞、T细胞、NK细胞、树突状细胞、血管和淋巴管、癌症相关成纤维细胞以及ECM的组成部分。
在转移性肿瘤中,TME中的免疫细胞环境和免疫调节受体的表达受到更多的免疫抑制。
当前和新兴的转移性疾病治疗策略
A) 对于转移性疾病的治疗,存在三种不同的情况。
首先,当转移性疾病在(新)辅助治疗环境中被疑为微转移性疾病时,由于其无法通过标准成像和筛查技术进行检测,因此具有较大的治疗难度。尽管多器官大转移在大多数情况下是不可治愈的,但我们仍可以采用选择性局部治疗来应对寡转移疾病,这可以在一定程度上延长患者的寿命,有时甚至可以治疗多种癌症。对于多器官转移性疾病,我们通常采用全身治疗方法,包括化疗、靶向治疗(如小分子抑制剂、抗体或抗体-药物偶联物)以及免疫疗法。
B) 我们需要强调以癌症细胞或其肿瘤微环境(TME)为靶点的治疗模式的重要性,以最大程度地消除转移细胞。
在微转移中,肿瘤细胞与免疫监测之间处于动态平衡状态。增殖的癌细胞经常被组织驻留或循环的免疫细胞清除,而处于休眠状态的癌细胞则能够逃避免疫系统的破坏。在寡转移中,较小的肿瘤会被TME中的驻留细胞以及募集的免疫细胞浸润。随着病情发展至多器官转移,TME的免疫抑制性会逐渐增强。

总结
转移是一个复杂的过程,它涉及到多个步骤和阶段。这些步骤和阶段可以灵活适应各种不断变化的情况,如细胞应激、细胞在组织微环境之外的生存、扩散、免疫逃避,以及与肿瘤微环境共同选择和最终器官定植。
随着科技的进步,单细胞图谱、谱系追踪和各种复杂的临床前及离体模型等新技术不断涌现。当前的主要挑战是确定转移的依赖性,这些依赖性可以根据患者的异质性或生物标志物进行定义。总的来说,转移研究和临床药物开发领域的重大进展有望改善转移性癌症患者的治疗效果。
扫描下方二维码
即可免费获取肿瘤转移信号通路合集海报


参考文献:Gerstberger S, Jiang Q, Ganesh K. Metastasis. Cell. 2023 Apr 13;186(8):1564-1579. doi: 10.1016/j.cell.2023.03.003
加入社群


关于福麦斯









